
编者按
2024年11月15日,第75届美国肝病研究学会(AASLD)年会在美国加利福尼亚州圣迭戈开幕,来自世界各地的肝病学家和从事肝病研究的专业人士齐聚一堂,分享探讨肝病学领域的突破性研究成果、新的治疗指南以及最新的治疗进展。在本届大会上,北京大学第一医院徐小元/于岩岩教授团队共有5项研究被收录,其中1项为大会口头报告,4项为壁报交流。值得一提的是,此次口头报告的内容是一项多中心、前瞻性临床试验,评估了索磷布韦维帕他韦 (SOF/VEL)联合预防性使用富马酸丙酚替诺福韦(TAF)治疗慢性HBV/HCV合并感染患者的疗效和安全性。研究结果显示,该治疗方案不仅能显著降低患者的HCV RNA水平,有效改善肝功能,而且在合并代偿期肝硬化的患者中,还能明显改善肝纤维化指标。更令人振奋的是,预防性使用TAF能在一定程度上预防HBV再激活,为患者提供了更安全、有效的治疗选择。
研究成果•精华速递点击上方链接查看原文及采访视频
研究一 SOF/VEL及TAF预防性用药在慢性HBV/HCV合并感染患者中的安全性和有效性:一项多中心研究
蔺宁博士在AASLD 2024现场报告
研究背景
HBV和HCV感染是全世界慢性肝病的主要病因。根据世界卫生组织2015年的统计,全世界有2.4亿人感染了HBV,7100万人感染了HCV。由于HBV和HCV具有相同的传播途径,HBV/HCV合并感染(HBV/HCV双重感染)在世界各地广泛存在,其患病率与HBV和HCV患病率密切相关。HBV/HCV合并感染比单纯HBV或单纯HCV感染更复杂。HCV可通过其核心蛋白、NS2和NS5A蛋白抑制HBV/HCV合并感染患者HBV复制。目前,直接抗病毒药物(DAAs)疗程短,持续病毒应答(SVR)率高,不良反应(AEs)发生率低,开创了慢性丙型肝炎治疗的新时代。但对于HBV/HCV合并感染患者,DAAs抗HCV治疗可导致HBV复制和蛋白表达增加,增加HBV再活化的风险。因此,本研究将评估SOF/VEL在中国HBV/HCV合并感染患者中的安全性和有效性,并评估TAF在直接抗病毒药物治疗期间对HBV再活化的预防作用。
研究方法
本研究是一项多中心、前瞻性、开放性临床试验。研究纳入2021年5月-2023年11月来自中国16家中心的83例HBV/HCV合并感染患者。患者根据是否伴有代偿期肝硬化分为两组,组1为无肝硬化的患者(n=64),组2为伴有代偿期肝硬化的患者(n=19)。所有患者将接受TAF预防性治疗4周,之后接受SOF/VEL治疗12周。组1患者如果治疗期间没有发生HBV再活化,将在第28周结束时停止访视。组2受试者将接受TAF治疗至第64周。研究访视点如下:筛查期(D0),TAF预防性治疗期(D1),SOF/VEL治疗期(W4、W8、W12、W16)和SOF/VEL治疗后期,即组1患者停止使用TAF结束时(W28)和组2患者停止使用TAF结束时(W64)。

图1. 研究设计图
研究的主要观察终点为停止SOF/VEL治疗后12周,HCV RNA<最低检测下限(Lower limit of quantification,LLOQ)的患者比例(SVR12),和导致研究药物停用的不良事件(Adverse events,AEs)。次要观察终点包括HBV DNA、HCV RNA、肝功能指标(ALT,AST,ALP,TBIL,ALB)、凝血功能指标(PLT)、肝纤维化指标(LSM,APRI,FIB-4),和HBV再激活的患者比例。计量资料使用XS和M(IQR)表示。组间比较采用独立样本t检验或非参数检验。组内比较采用配对t检验或非参数检验。P<0.05为差异具有统计学意义。
研究结果
83例HBV/HCV合并感染患者年龄为51(18.0)岁,HCV RNA为5.9 (1.7) log10 IU/mL。组1和组2患者HCV RNA分别为6.2 (1.5) log10 IU/mL和5.7 (1.8) log10 IU/mL,差异无统计学意义。组2患者ALT、AST、ALP、TBIL、LSM、APRI、FIB-4水平均高于组1,ALB、PLT水平低于组1。多数患者HCV基因型为1型,占比26.5%(图2)。
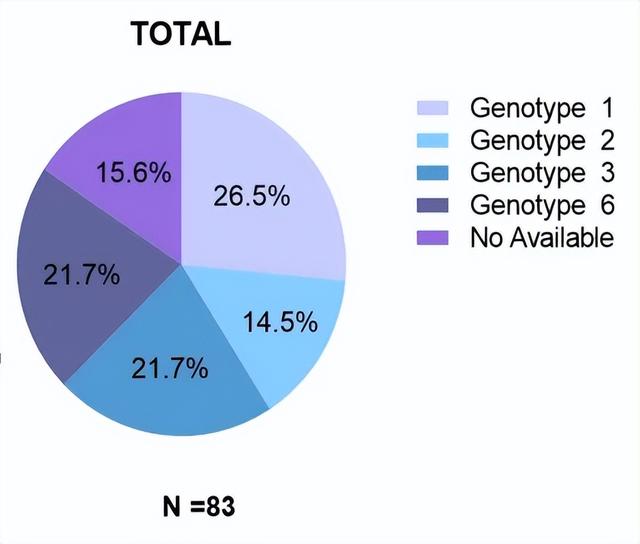
图2.患者HCV基因型分布
SOF/VEL治疗期结束时,总体SVR12为97.6%,其中组2 患者SVR12为100%(图3)。同时,所有患者HCV RNA 和 HBV DNA 水平均显著下降。比较两组患者治疗前后的肝功能和凝血指标变化(图4),组1患者ALT(41.4 vs. 17.0,P<0.001)、AST(38.0 vs. 22.0,P<0.001)、TBIL(14.3 vs. 13.6,P=0.006)水平下降,ALB(42.4 vs. 45.1,P<0.001)水平上升;组2患者ALT(59.0 vs. 22.0,P<0.001)、AST(60.0 vs 26.0,P<0.001)水平下降,ALB(41.3 vs. 42.5,P=0.002)、PLT(114.0 vs. 127.2,P<0.001)水平升高。组2患者肝纤维化指标(图5),即LSM(19.4 vs. 6.7,P=0.003)、APRI(1.6 vs. 0.6,P=0.007)和FIB-4(4.3 vs. 1.3,P=0.004)在治疗后均显著下降。

图3. SOF/VEL治疗后不同基因型的SVR12

图4. 肝功能和凝血指标变化

图4. 肝纤维化指标变化
研究过程中只有1位患者出现HBV再激活,该患者的HCV基因型为3型。该患者的HBV DNA水平在筛查期和TAF预防性治疗期均低于LLOQ,在SOF/VEL治疗结束时,HBV DNA水平升高至2.15 log10 IU/mL,但随后又恢复至低于LLOQ的水平。研究过程中未出现导致药物停用的不良事件。
研究结论
SOF/VEL可明显降低HBV/HCV合并感染患者的HCV RNA水平,改善其肝功能,安全性较高。合并代偿期肝硬化的患者在接受抗病毒治疗后,其肝纤维化指标(LSM、APRI和FIB-4)也有明显改善。此外,HBV/HCV合并感染患者预防性使用TAF可在一定程度上预防HBV再激活。
研究二 多烯磷脂酰胆碱改善非慢性乙型肝炎患者肝功能的疗效:一项真实世界研究蔺宁 , 徐京杭 , 韩一凡 , 曾湛 , 于岩岩 , 徐小元*
北京大学第一医院

研究目的
多烯磷脂酰胆碱(PPC)注射液是临床中常用的肝损伤治疗药物,广泛用于治疗各种病因的肝损伤。我们先前已报道过PPC注射液降低慢乙肝患者ALT和AST与还原型谷胱甘肽及异甘草酸镁疗效相当的真实世界研究结果。本研究旨在进一步探究PPC注射液对不同病因的非慢乙肝患者的疗效,并评价PPC的剂量效应。
研究方法
患者数据收集自全国多中心注册数据库。该数据库收集了2018年10月至2019年9月中国16个省264家医院的住院数据。肝功能异常且至少有一次PPC治疗后肝功能指标随访结果的患者被纳入到本次分析队列。排除慢乙肝患者以及同时合并其他护肝药物治疗的患者。共有1454例患者符合纳入条件。评估指标包括ALT、AST、GGT、总胆红素、凝血酶原活动度(PTA)、球蛋白和白蛋白。采用线性混合增长曲线分析的方法,比较经年龄和性别协变量调整后肝功能指标变化斜率的差异。此外还比较了PPC不同剂量组的疗效差异。P<0.05为差异有统计学意义。
研究结果
1454例患者的中位年龄为52岁,63.8%为男性。在全部患者队列中,PPC治疗显著降低患者ALT(每天下降9.0 U/L,P<0.001),AST(每天下降7.0 U/L,P<0.001)和总胆红素水平(每天下降0.9 μmol/L/,P<0.001)。PPC治疗后,患者白蛋白水平升高(每天升高0.7 g/L,P<0.001)。
药物性肝损伤(DILD)患者的基线ALT水平相比非DILD患者更高(P<0.05)且下降速率更快(P<0.05)。肝硬化患者的ALT(P<0.05)和AST(P<0.05)基线水平较非肝硬化患者低,且治疗期间下降速率慢。自身免疫性肝病患者与非自身免疫性肝病患者相比,ALT及AST恢复水平相近。酒精性肝病(ALD)患者接受PPC治疗后,GGT下降速率相比其他病因患者更快(P<0.001)。
剂量效应分析表明基线ALT水平越高的患者接受PPC治疗的剂量越大。在不同治疗剂量组中,患者ALT水平恢复正常的时间相近(2、3、4和6-8瓶组分别为11.4、10.2、11.3和11.9天)。
研究结论
自身免疫性肝病和非肝硬化患者经PPC治疗后,ALT和AST水平均有较快下降。DILD患者的ALT水平和ALD患者的GGT水平的下降速率较其他肝病患者更为明显。基线ALT越高的患者接受PPC治疗剂量越大。在不同剂量组中,患者ALT水平恢复正常时间相近。

研究三

研究四和研究五
