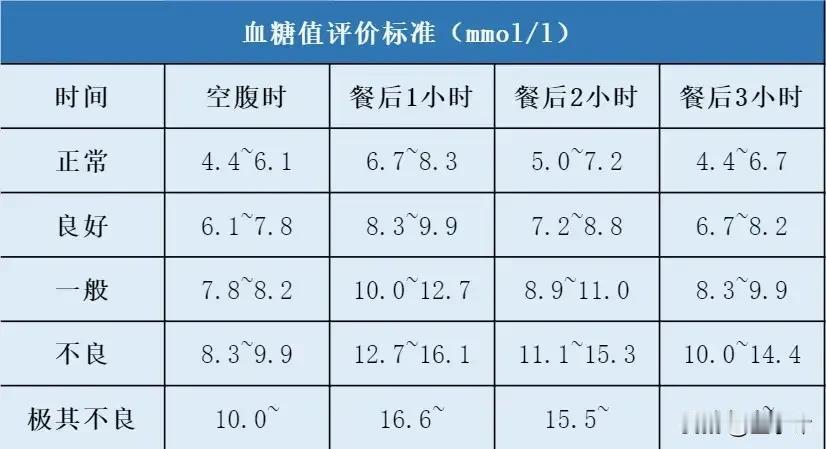
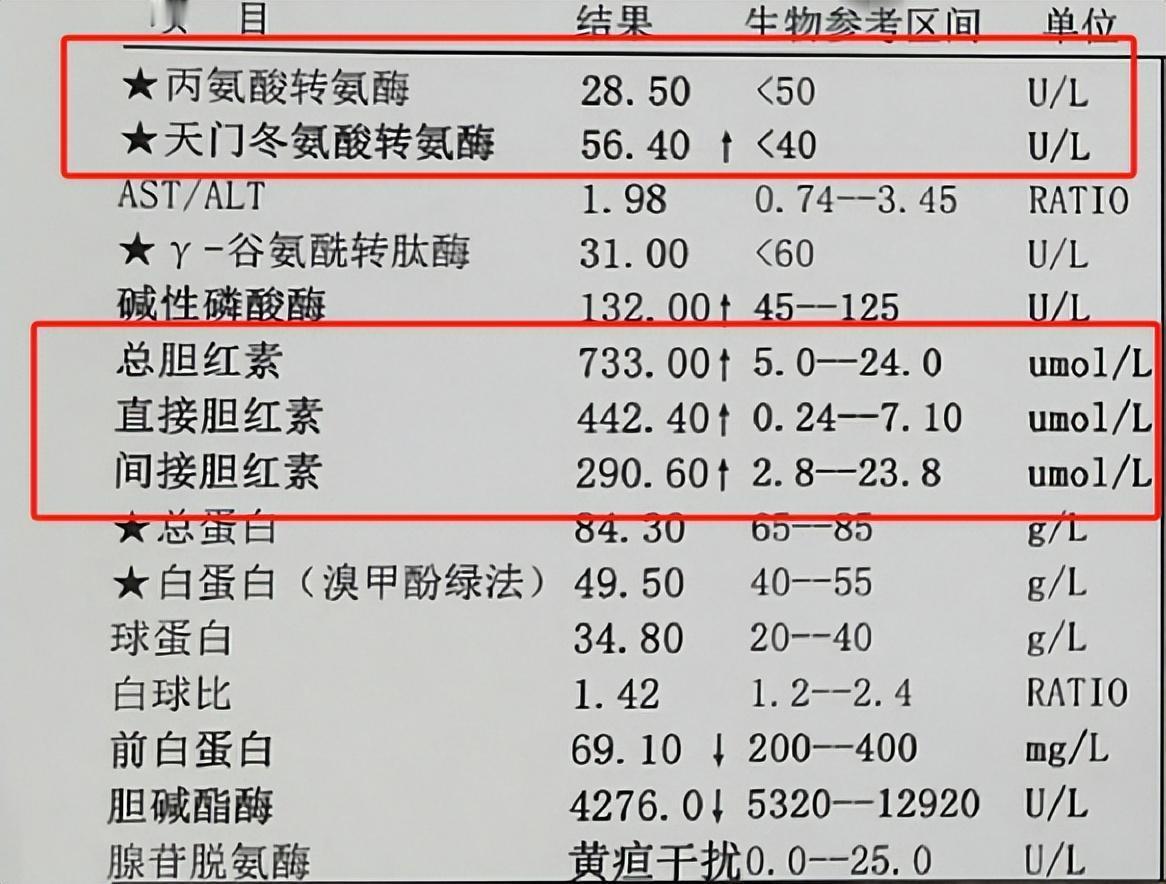
治肾药物伤肾,并不少见,比如治疗肾小球疾病的猛药:环孢素和他克莫司,具有一定的肾毒性,有概率引起新的肾脏损伤。
不过环孢素和他克莫司毕竟属于“猛药”,有副作用也见怪不怪了。当医生决定使用环孢素和他克莫司时,肾脏损伤的进展速度往往已经踏上了高速,即便有概率在未来引起新的肾脏损伤,也得先把眼下的急症解决了。所谓重病下猛药,莫不如此。
然而,我们万万没想到,最近,一向以温和著称的RAS抑制剂(也就是普利/沙坦类药物),也暴露出了肾毒性!
普利/沙坦,这可是指南推荐了二三十年、以副作用小著称、肾内科处方量最大的药物。它进入肾内科的时候,笔者还没进入肾内科呢!
这肾毒性是怎么回事呢?
近日,Circulation Research(《循环研究》)的封面文章,报道了RAS抑制剂导致肾脏成为病理性(肾小动脉肥厚、纤维化)器官的机制。
研究发现,当长期应用普利/沙坦后,会出现肾小动脉肥厚。

肾小动脉是哪里呢?
看我手边这个肾小球模型,进出肾小球的血管,就是肾小动脉,我画的这个红圈:

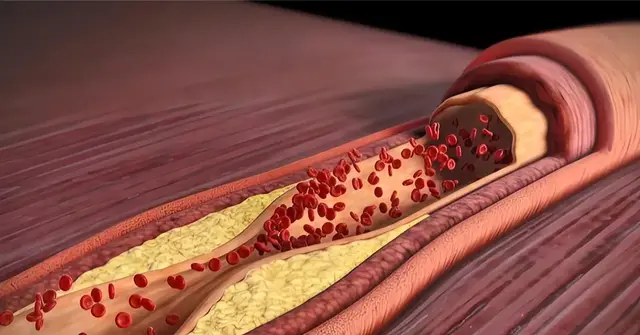
动脉血管发生肥厚,管腔就窄了,血液流不动了,血液中的毒素也就排不出去了!于是,会出现肾功能下降。
普利/沙坦是怎么伤肾的呢?
这个机制比较复杂、反应链条也比较长,我长话短说。
简单来说:普利/沙坦阻断了肾素的作用,于是肾素细胞大量增生,神经生长因子分泌增加,激活交感神经,交感神经回过头来又进一步刺激肾素细胞增生,形成「神经-免疫-内分泌改变」这样一个恶性循环。
形象点说:肾脏想要升压了(分泌肾素),这时咱们拿降压药把肾脏的血压降下去了。肾脏它能服气吗?不服气,于是肾脏大量增殖升压细胞(肾素细胞),想要把压力再次加回来,即便是以肾功能衰退为代价也在所不惜。
不得不说,肾脏的意志真是够坚定的。
遥想当年原始社会,咱们的祖先在野外遭受重创/中毒后,肾脏开启升压开关,开足肾功能的功率,保障全身的重要器官供血、供应干净的血,才让呼吸心跳延续下去。虽然肾脏寿命减少了,但是人活下来了,起码能活到繁衍后代的年龄。
可以说,没有肾脏的自我牺牲机制,就没有人类繁衍至今。
如今,人类有了安全的生活环境、充分的医疗保障,不需要肾脏这种自残式的牺牲了。
可是几百万年演化出的生理机制,已经刻进了基因里,哪里是我们几十年里能改变的,肾脏依然不肯放弃它的自我牺牲——即便我们用药物来帮助它。
这也解释了,为什么普利/沙坦改善肾功能的幅度并不大,在各种基础药物中并不突出。
不过,普利/沙坦类药物仍然是有用的:消除了眼下的一个大麻烦(肾小球内压升高),换来了未来的一个小一些的麻烦(肾脏的反抗:肾小动脉增厚)。
这算是肾毒性吗?
也算是吧。每一种肾毒性药物的使用,都有它利大于弊的理由。只要益处大于弊端,普利/沙坦依然具有减轻肾损伤的作用。
只是如今新型药物越来越多,肾功能保护作用超越普利/沙坦的药物也不罕见了。它不再像以前是肾科明星,更多地是作为辅助药物,继续在它的岗位上履行职责、发光发热。