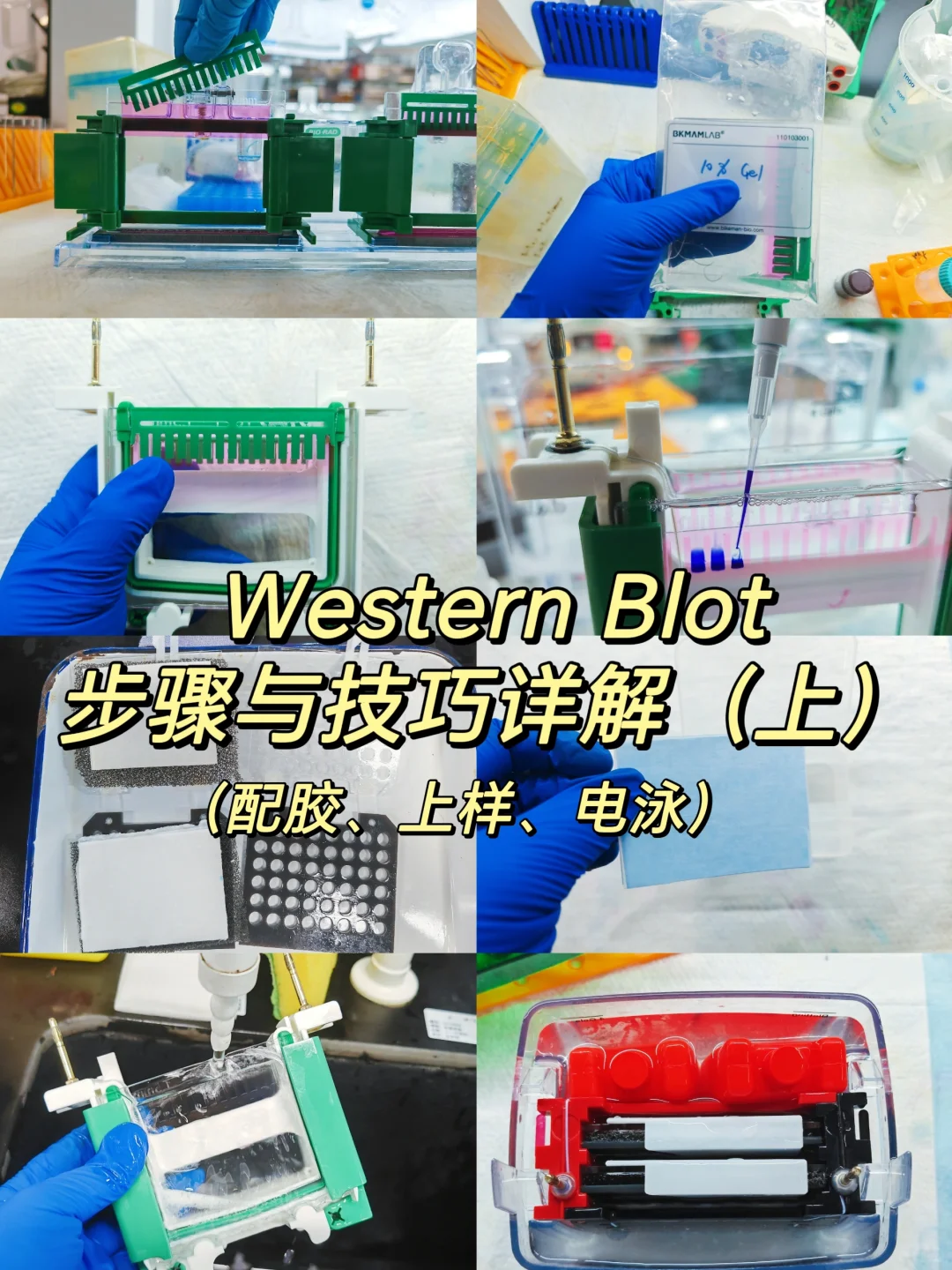
蛋白质免疫印迹(Western Blot, WB)是一种检测特定蛋白表达量的实验。以下是简要的实验步骤(详细步骤和操作见图):
1. 配置SDS-PAGE胶
10%分离胶:混合ddH2O 7.9ml、30%丙烯酰胺6.7ml、1.5M Tris-HCl pH 8.8 5.0ml、10% SDS 200μl、10% 过硫酸铵200μl和四乙基乙二胺8μl,倒入玻璃板中,静置凝固。
浓缩胶:混合ddH2O 4.1ml、30%丙烯酰胺1.0ml、1.0M Tris-HCl pH 6.8 0.75ml、10% SDS 60μl、10% 过硫酸铵60μl和四乙基乙二胺6μl,倒入已凝固的分离胶上,插入梳子。
2. 蛋白质电泳SDS-PAGE
电泳液:按Tris 3.03g、甘氨酸18.77g、SDS 1g和ddH2O 1000mL比例配置。
上样:拔出梳子,向孔中加入蛋白样品或marker。
电泳:恒压80V启动,蛋白进入分离胶后调至120V,电泳至适当位置停止,以自己需要的最小蛋白没有跑到底为准。
3. 湿转法转膜
转膜液:1×转膜液由100ml 10×转膜液(Tris 3.03g、甘氨酸18.77g和ddH2O 1000mL)、200ml无水甲醇和700ml ddH2O配置。
激活PVDF膜:在醇类中浸泡至半透明。
转膜:将凝胶转移到三明治夹上,覆盖激活的PVDF膜,冰上300mA恒流转膜120分钟(具体时间根据分子量大小调整)。
4. 封闭及抗体孵育
TBST:由10×TBS(Tris 24.23g,NaCl 80.06g,ddH2O 1000ml)、去离子水、吐温和适量盐酸配置,调节至pH约7.4。
封闭:PVDF膜浸泡于含5%BSA或脱脂奶粉的TBST中1小时。
一抗孵育:TBST洗涤后,浸泡于一抗中,4℃过夜。
二抗孵育:TBST洗涤,配置含5%BSA或脱脂奶的TBST二抗,室温孵育1小时,TBST洗涤。
5. 化学发光检测
化学发光液:A液和B液按1:1混合,均匀淋于膜表面。
曝光:将膜放置于化学发光仪中,根据需要调整曝光时间。


































我就在这蹲住了,开始学习!
您好,请问一下Marker和内参怎么用呀
为什么是用脱脂奶配二抗?我们实验室里是用tbst配的二抗,有什么区别吗?