🔑 Western Blot的图最后会得到白色背景上的黑色条带,条带越黑说明蛋白量越多。一般来说好看的条带就是该黑的地方黑、该白的地方白。所以优化WB的图就应该从这个角度考虑,来优化步骤。
📝 样本制备
1⃣ 充分裂解:确保样本彻底裂解,以释放所有蛋白质。使用物理方法(如超声)和化学方法(如含有SDS的裂解液)。
2⃣ 去除杂质:通过离心去除未裂解的细胞碎片和未被裂解的蛋白质,以减少电泳过程中的杂质。
3⃣ 蛋白酶抑制剂:添加蛋白酶抑制剂以防止蛋白降解。
4⃣ 准确定量:使用BCA等方法准确测定蛋白浓度,确保每个泳道的蛋白量一致。
🌐 SDS-PAGE电泳
1⃣ 凝胶浓度:根据目标蛋白的分子量选择合适的凝胶浓度。大分子量蛋白通常使用4%-6%的凝胶。中等分子通常使用8%-10%的凝胶,小分子通常使用12%-15%的凝胶。如果目标蛋白的分子量范围较宽,可以考虑使用梯度凝胶。
2⃣ 上样缓冲液:使用新鲜的上样缓冲液,并确保样品与上样缓冲液充分混合后变性。
3⃣ 调整上样量:如果蛋白表达量低,可以增加上样量。
🔄 转膜
1⃣ 转膜条件:优化转膜时间、电压和缓冲液,特别是对于大或小分子量的蛋白,确保蛋白质有效转移至膜上。
🚫 封闭
1⃣ 封闭液:使用5%脱脂奶粉或BSA作为封闭剂室温封闭1小时。
2⃣ 封闭时间:可以考虑延长封闭时间以确保完全封闭。
🔬 抗体孵育
1⃣ 一抗选择:选择高特异性的一抗,并根据制造商的建议进行稀释,太高容易导致非特异性结合,太低会导致目标条带弱、背景黑。
2⃣ 二抗选择:选择与一抗宿主相匹配的二抗,并使用适当的标记。
3⃣ 抗体配置:使用BSA或专用的抗体稀释液配置抗体,具有一定的封闭作用。
4⃣ 孵育时间:一抗一般4℃过夜,二抗一般室温1小时。延长孵育时间和提高孵育的温度会有助于抗体和目标蛋白的结合,但是也容易导致更多的非特异性结合。
🧼 洗涤
1⃣ 洗涤次数:在一抗和二抗孵育后,充分洗涤以去除未结合的抗体。
2⃣ 洗涤液:使用TBST或其他洗涤液,添加吐温-20以减少非特异性吸附。
3⃣ 洗涤平衡:洗涤也不能过分,避免一抗和二抗被过度清洗。
📸 ECL显影
1⃣ 发光液现配现用:确保ECL试剂新鲜,避免影响显色效果。
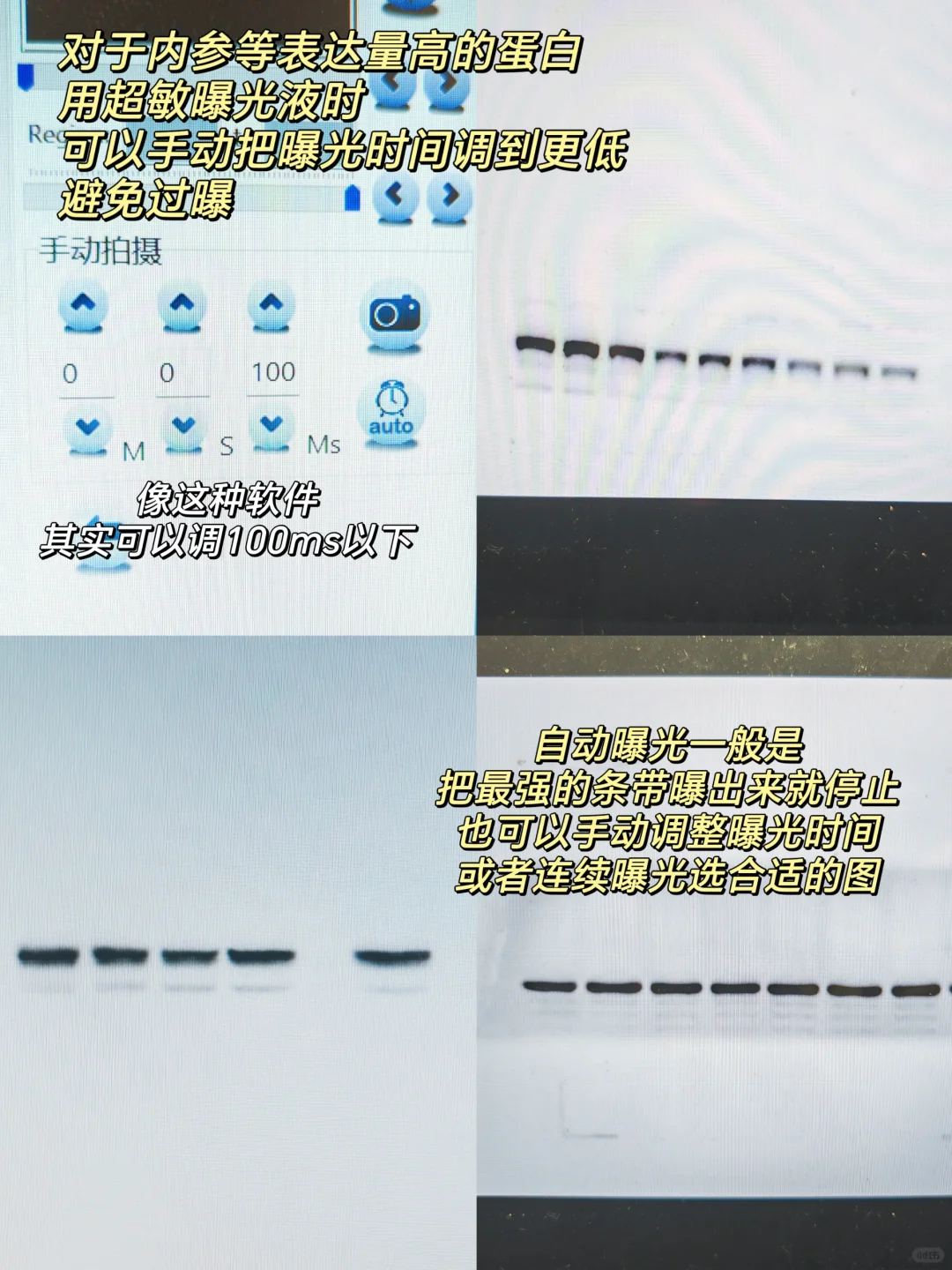
2⃣ 曝光时间:根据信号强度调整曝光时间,避免过曝导致条带过黑。
3⃣ 超敏检测:对于表达量低的蛋白可以使用超敏化学发光液和接触式化学发光仪。




























分子量15-20转膜条件是什么
感谢分享