每当我们谈论生育的时候,【妊娠纹】往往被刻画成女性的勋章,从而掩盖生育的代价。被忽视的伤痕,比分娩更痛,真正让女性「谈生色变」的,不是生育风险,而是无人理解。正视女性生育代价!我们先从妊娠纹说起,这种生育代价中一抹难以抹除的伤疤。
关于妊娠纹
女性怀孕后,随着胎儿一天天长大,肚子就像吹气球一样慢慢鼓起来。这时候,皮肤就得跟着一起“努力”地拉伸,好给肚子里的小宝宝腾出足够的空间。
但是,皮肤的弹性是有限的,它里面有种叫做弹性纤维和胶原纤维的东西,它们就像皮肤的“小弹簧”,平时负责让皮肤保持弹性和紧致。可当肚子撑得太大、太快时,这些“小弹簧”就有点受不住了,它们会开始断裂。

“小弹簧”断了以后就在皮肤上留下了痕迹,这些痕迹就是我们说的妊娠纹。
妊娠纹刚开始的时候,可能是粉红色或者紫红色的,有点像是皮肤下面的血管颜色透了出来。这是因为皮肤被拉伸得太厉害,血管也跟着变得明显了。随着时间的推移,这些颜色会慢慢变淡,最后变成银白色或者灰白色,就像是皮肤上的小细纹一样。

除了肚子上,臀部、大腿或者乳房周围也可能会长妊娠纹,均是因为这些地方的皮肤被拉伸得太厉害,弹性纤维和胶原纤维断裂了。
治疗妊娠纹,归其根源,是纤维组织发生了问题,最重要的还是需要修复组织里受伤、老化的细胞,让新的细胞生长出来。
随着医学与技术的发展,以及美容护肤科技的进步,也出现了更多更好的解决方案。
干细胞外泌体:妊娠纹修复的“潜力新星”
对付妊娠纹,目前已经有一些医疗美容手段,对已生成的妊娠纹会有些改善效果,例如光子色素、射频治疗、超声聚焦、点阵激光、微晶磨削等等。
除此以外,干细胞外泌体正在成为修复妊娠纹的新希望。
干细胞外泌体可以通过以下几种方式发挥作用:
1.促进皮肤成纤维细胞增殖和胶原蛋白合成:
外泌体含TGF-β、EGF、VEGF等生长因子,可刺激皮肤成纤维细胞增殖;其miRNA可以上调胶原蛋白合成基因;蛋白质和脂质参与促进皮肤成纤维细胞增殖和胶原蛋白合成的途径。
2.抑制皮肤成纤维细胞凋亡:
外泌体中的抗凋亡因子,如Bcl-2,它们能抑制皮肤成纤维细胞凋亡;外泌体能激活Akt和ERK等信号通路,这些通路也具有抗凋亡作用;外泌体中的miRNA也能下调促进凋亡的基因表达。
3.促进血管生成:
外泌体包含血管内皮生长因子(VEGF)和成纤维细胞生长因子(FGF),这些因子能刺激血管内皮细胞增殖和迁移。
4.抑制炎症:
发炎的组织通常会显得更红、更凸起,使其成为肥厚性疤痕和早期妊娠纹的显着特征。干细胞外泌体通过其抗炎作用,可以增加细胞外基质和生长因子的产生,从而改善皮肤的质量以及组织的愈合。

值得注意的是,上述方法并非单独运作,而是相互协作,共同促进肌肤健康状态的显著提升。干细胞外泌体在这一协同过程中扮演着关键角色,它微妙地平衡着胶原蛋白的促进、炎症的调节以及组织的再生。这种协同机制确保了受影响区域能够获得全面且持久的改善。随着胶原蛋白含量的增加、炎症的缓解以及组织再生进程的推进,皮肤正逐步迈向更加健康的状态。
干细胞外泌体针对妊娠纹修复的临床研究进展
临床研究一:
今年7月,发表在《Stem Cell Research&Therapy》的一篇文章给妊娠纹的治疗带来了巨大的惊喜。这是来自伊朗的一项随机临床试验,评估了人脐带间充质干细胞上清液(里面包含多种细胞因子、生长因子、蛋白质、外泌体等成分),加微针疗法与单纯微针疗法对妊娠纹的疗效。

作者通过这项随机、双盲临床试验纳入了10名年龄在18至60岁之间且腹部妊娠纹的女性。经过初步评估后,为每位患者选择了一个病变部位。所有被选中的妊娠纹都被鉴定为白纹。每个妊娠纹被分成两等份。通过随机分配,一边接受微针治疗和皮内注射间充质干细胞上清液组,另一边接受微针治疗和皮内注射生理盐水作为对照组。
每位患者在干预开始前和最后一次治疗后三个月接受检查,其结果显示如下:
①医生评估:
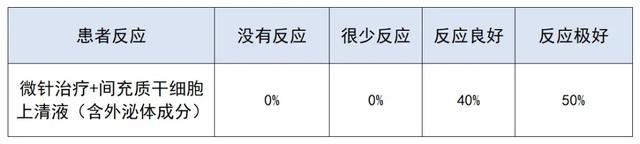
医生评估表明,在微针干细胞上清液组中,有40%和50%的患者反应分别为良好和极好。没有受试者表现出很少或没有反应。微针干细胞上清液组的医师满意度显著高于微针生理盐水组。
②三个月后患者自我评估:

根据患者自我评估,微针干细胞上清液组中40%和60%的患者在干预后三个月分别认为其病变反应良好或极好。与医生的评估一致,与微针生理盐水组相比,微针干细胞培养基组的患者满意度显著更高。
临床研究二:
2021年,一项发表在《Pharmacol Res》的关于外泌体在皮肤病学中的新机制和应用文献也指出:内源性多种外泌体是塑造皮肤生理和病理发育的关键协调器。此外,外源性外泌体,如干细胞外泌体,可以作为修复、再生和恢复皮肤组织活力的新治疗选择。

该研究的作者指出,来自干细胞和其他细胞类型的外泌体可以作为再生医学和美学的治疗选择,特别是在预防和减少疤痕、调节色素沉着、面部年轻化和头发生长方面。
临床研究三:
2018年第四军医大学西京医院烧伤皮肤外科的研究人员在国际科技期刊《Exp Cell Res.》上发表题为“Cell-free therapy based on adipose tissue stem cell-derived exosomes promotes wound healing via the PI3K/Akt signaling pathway”(基于脂肪组织干细胞衍生的外泌体的无细胞疗法通过PI3K/Akt信号通路促进伤口愈合)的研究论文。
研究结果显示,ADSC衍生的外泌体被成纤维细胞吸收,与未经外泌体处理的细胞行为相比,其在细胞增殖和迁移方面表现出显着的剂量依赖性增加。更重要的是,在外泌体刺激后,成纤维细胞中I型胶原蛋白(Col 1)、III型胶原蛋白 (Col 3)、MMP1、bFGF和TGF-β1的mRNA和蛋白质水平均增加。
干细胞外泌体疗法为妊娠纹的治疗带来了革命性的突破。相较于传统疗法,该疗法无需手术介入,也无需承受外科手术可能带来的切割、麻醉需求及漫长的康复期,它依据个性化疗法,采取局部涂抹或临床注射的方式。此外,干细胞外泌体疗法摒弃了合成化学品的依赖,转而利用人体内在的再生潜能,激发并加速身体的自然修复过程,这一理念与人体固有的自我恢复和再生能力相契合。
当前,外泌体在护肤领域的潜力正日益凸显。随着临床研究的不断推进,医学专家正逐步积累更多关于外泌体安全性和有效性的科学证据,这将为外泌体护肤产品的创新开发与广泛应用奠定坚实基础。
参考资料:
[1]Wang L, Hu L, Zhou X, Xiong Z, Zhang C, Shehada HMA, Hu B, Song J, Chen L. Exosomes secreted by human adipose mesenchymal stem cells promote scarless cutaneous repair by regulating extracellular matrix remodelling. Sci Rep. 2017 Oct 17;7(1):13321. doi: 10.1038/s41598-017-12919-x. Erratum in: Sci Rep. 2018 May 1;8(1):7066. doi: 10.1038/s41598-018-24991-y. Erratum in: Sci Rep. 2021 Feb 1;11(1):3245. doi: 10.1038/s41598-021-82225-0. PMID: 29042658; PMCID: PMC5645460.
[2]Behrangi E, Feizollahi M, Zare S, Goodarzi A, Ghasemi MR, Sadeghzadeh-Bazargan A, Dehghani A, Nouri M, Zeinali R, Roohaninasab M, Nilforoushzadeh MA. Evaluation of the efficacy of mesenchymal stem cells derived conditioned medium in the treatment of striae distensae: a double blind randomized clinical trial. Stem Cell Res Ther. 2024 Mar 5;15(1):62. doi: 10.1186/s13287-024-03675-7. PMID: 38439103; PMCID: PMC10913631.
[3]Xiong M, Zhang Q, Hu W, Zhao C, Lv W, Yi Y, Wang Y, Tang H, Wu M, Wu Y. The novel mechanisms and applications of exosomes in dermatology and cutaneous medical aesthetics. Pharmacol Res. 2021 Apr;166:105490. doi: 10.1016/j.phrs.2021.105490. Epub 2021 Feb 12. PMID: 33582246.
[4]Zhang W, Bai X, Zhao B, Li Y, Zhang Y, Li Z, Wang X, Luo L, Han F, Zhang J, Han S, Cai W, Su L, Tao K, Shi J, Hu D. Cell-free therapy based on adipose tissue stem cell-derived exosomes promotes wound healing via the PI3K/Akt signaling pathway. Exp Cell Res. 2018 Sep 15;370(2):333-342. doi: 10.1016/j.yexcr.2018.06.035. Epub 2018 Jun 28. PMID: 29964051.
