研究背景
自由基中间体是单电子未配对的化学物质,因其在有机合成中的独特反应性,被广泛应用于药物研发、材料科学和精细化工等领域。与传统的双电子(极性)化学方法相比,自由基反应具有反应路径独特、官能团兼容性高等优点。然而,自由基中间体反应活性过高,难以控制,且传统生成自由基的方法通常需要危险的试剂、剧毒金属或苛刻的反应条件,这为自由基化学的进一步发展带来了巨大的挑战。
成果简介
为了解决这一问题,英国曼彻斯特大学Huaibo Zhao, Valentina Dafnae Cuomo,Ciro Romano & David J. Procter等人在Nature Reviews Chemistry期刊上发表了题为“Light-assisted functionalization of aryl radicals towards metal-free cross-coupling”的最新综述。
该团队综述了近年来光催化生成芳基自由基用于C(sp²)−C(sp²)、C(sp²)−C(sp³)及C(sp²)−C(sp)键构建的研究进展,总结了利用可见光温和条件下生成芳基自由基的多种策略,包括直接光激发、单电子转移、能量转移催化以及电子供体–受体(EDA)复合物机制等。在此基础上,研究者们提出了无金属光催化交叉偶联的新方法,通过选择性激发芳基自由基前体,显著提高了反应选择性与效率,同时拓展了适用的底物范围与自由基前体种类。
利用这种光辅助无金属策略,该团队成功实现了高选择性的芳基自由基加成、氢原子转移及卤素原子转移反应,显著提高了交叉偶联反应的性能。此外,这些光生成的芳基自由基还可与其他催化体系(如有机催化)联用,为开发不对称反应和可持续有机合成技术提供了新思路。

研究亮点
(1)综述了光催化生成芳基自由基的最新进展,得到了芳基自由基在无金属交叉偶联反应中的重要应用。研究表明,通过可见光的激发,可以在温和条件下生成芳基自由基,采用了多种策略,如直接光激发、单电子转移(SET)、电子供体-受体(EDA)复合物和能量转移催化(EnT)。这些方法不仅提高了反应的选择性,还在一定程度上避免了传统方法的安全隐患。
(2)文章重点讨论了芳基自由基在光催化无金属协议中的应用,并阐明了芳基自由基如何用于构建C−C键,尤其是C(sp2)−C(sp2)、C(sp2)−C(sp3)和C(sp2)−C(sp)键。研究表明,芳基自由基能够参与多种机理途径,包括与π体系的加成、氢原子转移(HAT)和卤素原子转移(XAT)。此外,采用光催化条件生成芳基自由基时,使用了大量稳定的前体,并且新型前体的设计和开发仍在持续推进。这些研究为扩展芳基自由基的合成应用,尤其是实现不对称反应提供了新的可能性。
图文解读

图1: 芳基自由基中间体的光诱导交叉偶联反应概述。
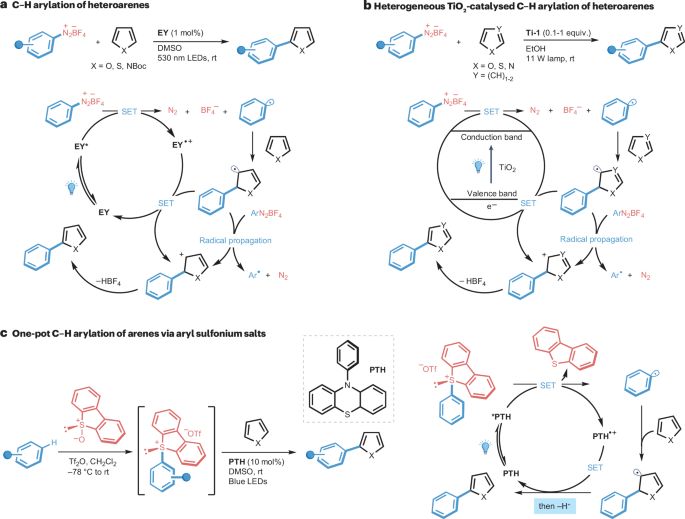
图2:芳基自由基中间体的杂芳族化合物光催化芳基化。
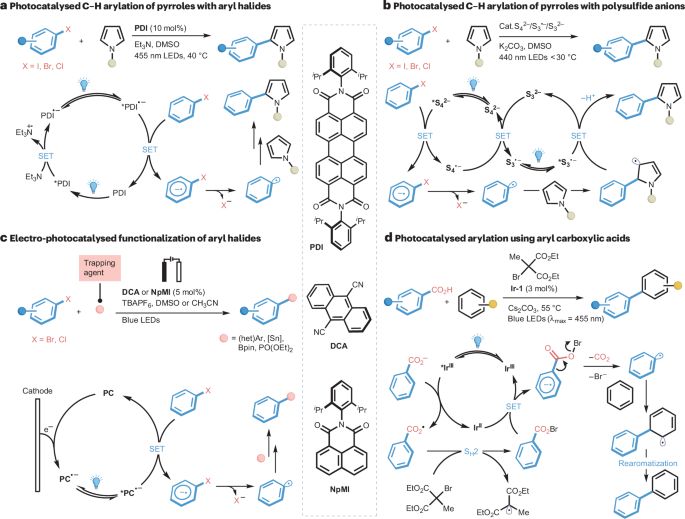
图3:以芳基卤化物和羧酸作为芳基自由基前体,(杂)芳烃的光催化芳基化。

图4:芳基自由基中间体的光催化无金属烯基化、炔基化和羰基化反应。

图5:通过将芳基自由基中间体加成到烯烃上,构建新的C(sp2)–C(sp3)键。
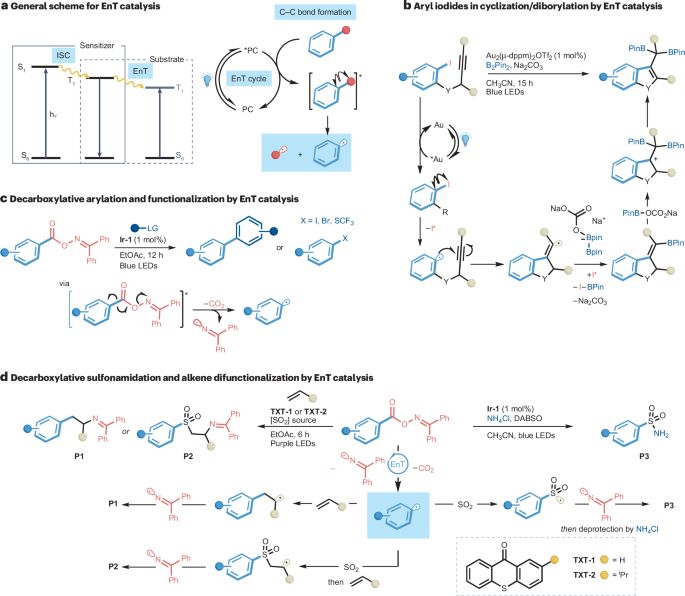
图6: 通过ENT催化产生了芳基自由基的光催化功能化。

图7: EDA配合物产生的芳基自由基的光催化功能化。
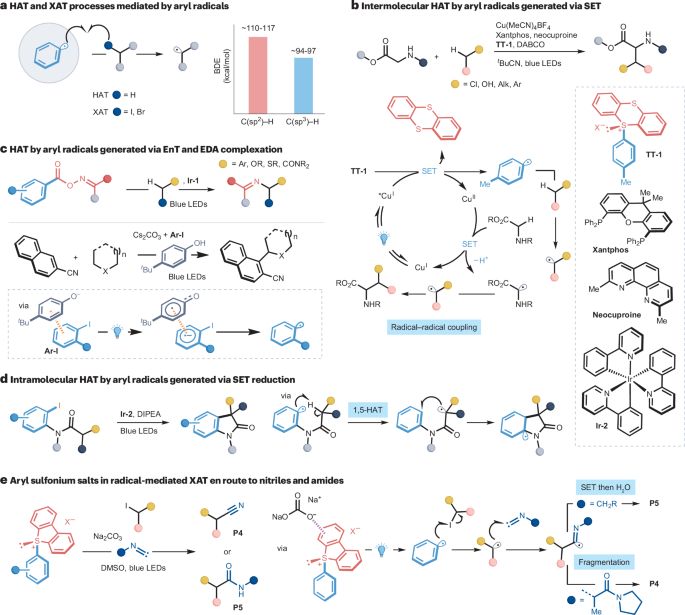
图8: 芳基自由基介导HAT和XAT的光辅助交叉偶联反应。
结论展望
光辅助的芳基自由基生成方法不仅拓宽了传统交叉偶联反应的应用范围,还为实现无金属催化的高效反应提供了新的途径。通过光激发,芳基自由基可以在温和的条件下从多种稳定前体中生成,避免了传统方法中对金属催化剂的依赖。
这种方法不仅提高了反应的选择性和安全性,还为芳基自由基的应用开辟了新的方向,尤其是在激活通常不反应的底物时。文章指出,虽然芳基自由基的应用仍在不断发展,特别是在氢原子转移(HAT)和卤素原子转移(XAT)等反应中,但这一领域仍然蕴藏着巨大的潜力。
未来,结合有机催化剂或其他激活方法(如电化学)可能进一步拓展芳基自由基的合成应用,特别是在不对称反应和更复杂的反应体系中。因此,深入研究芳基自由基的生成机理和反应特性,将为未来的合成转化提供更加精确的工具,推动新型绿色合成方法的发展。
文献信息
Zhao, H., Cuomo, V.D., Tian, W. et al. Light-assisted functionalization of aryl radicals towards metal-free cross-coupling. Nat Rev Chem (2024).
